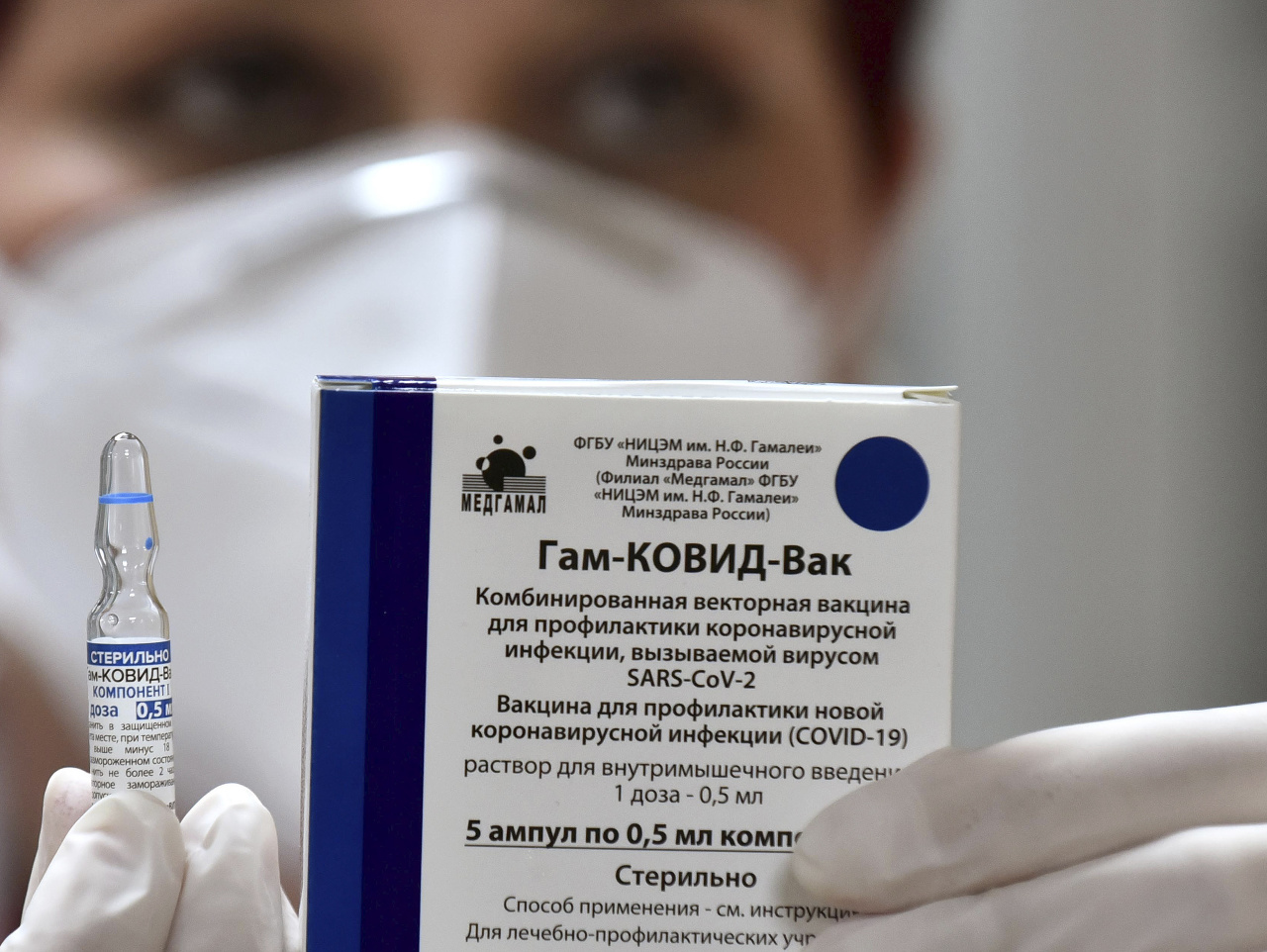
PRAHA - Pokým Rusi tvrdia, že žiadosť o registráciu vakcíny Sputnik V v Európskej únii podali, Európska lieková agentúra (EMA) podľa svojich vyjadrení žiadnym takýmto dokladom nedisponuje. Ako je to možné? Zdá sa, že pravda je zase raz niekde uprostred. Ruský investičný fond RDIF, ktorý vývoj platil, na twitteri naznačil, že žiadosť podal u iného orgánu. Dôvod, prečo sa fond neobrátil priamo na EMA, však nie je jasný.
Boj s KORONAVÍRUSOM v plnom prúde: Aktuálny PREHĽAD vakcín, ktoré majú svetu pomôcť zvíťaziť!
Európska lieková agentúra je od roku 2015 jediným orgánom, ktorý má mať na starosti schvaľovanie liekov v celej EÚ. Ruský investičný fond RDIF však napriek tomu mal podať žiadosť o registráciu na HMA, združenie šéfov jednotlivých štátnych liekových agentúr v Európskom hospodárskom priestore, ktoré neprestalo existovať a je naďalej aktívne. Podľa portálu novinky.cz rieši v spolupráci s EMA aj otázky vakcín proti covidu-19. Činnosť HMA má pokračovať z dôvodu, že Európsky hospodársky priestor sa úplne neprekrýva s EÚ. Okrem 27 krajín EÚ sú členmi HMA aj Nórsko, Island, Lichtenštajnsko a Veľká Británia.
RDIF CEO Kirill Dmitriev: We have received numerous requests from EU states to provide #SputnikV directly to them based on the reviews of their national agencies. We will continue to do so as well as work with EMA based on the rolling review procedure we initiated in January.
— Sputnik V (@sputnikvaccine) March 1, 2021
Z vyjadrenie RDIF na Twitteri vyplýva, že už v minulosti rokoval s Európskou liekovou agentúrou, preto nie je jasné, prečo sa so žiadosťou o registráciu neobrátil práve na ňu. "RDIF predložil žiadosť Európskej liekovej agentúre o vedecké posúdenie vakcíny Sputnik V 22. októbra 2020. Zástupcovia fondu, vedci, ktorí vyvinuli Sputnik V, a predstavitelia EMA mali vedeckú konzultáciu 19. januára." EMA agentúre RIA Novosti potvrdila, že konzultácie s tímom, ktorý vakcínu vyvinul, sa skončili a je možné podať žiadosť o registráciu.
Z celého tohto zmätku vyplýva niekoľko ďalších otázok. Okrem toho, prečo sa RDIF neobrátil priamo na EMA, sa natíska otázka, prečo HMA žiadosť neodmietla, keďže registrácia jej neprináleží, prípadne prečo túto žiadosť neposunila EMA, keď s ňou spolupracuje.
Situáciu však komplikujú aj výnimky. "V spoločnom vyhlásení EMA a HMA stojí, že podľa legislatívy EÚ patrí väčšina vakcín pod centralizovanú procedúru schvaľovania. Týka sa to vakcín vyrábaných biotechnologickými postupmi," uviedli novinky.cz. Medzi tie by zrejme bolo možné zaradiť aj Sputnik V, pretože využíva adenovírusový vektor rovnako ako vakcína od AstraZenecy, ktorú EMA schvaľovala.
Pre očkovacie látky, ktoré sú napríklad tvorené inaktivovanými či oslabenými vírusmi, však existujú aj iné možnosti schválenia. Môžu byť schválené len v jednej či viacerých krajinách EÚ. EMA a HMA vyzvali, aby tie úrady, ktoré umožnili ich schválenie v jednej alebo viacerých krajinách EÚ, tiež využili centralizovaný systém a zabezpečili rovnosť prístupu v rámci celej EÚ.