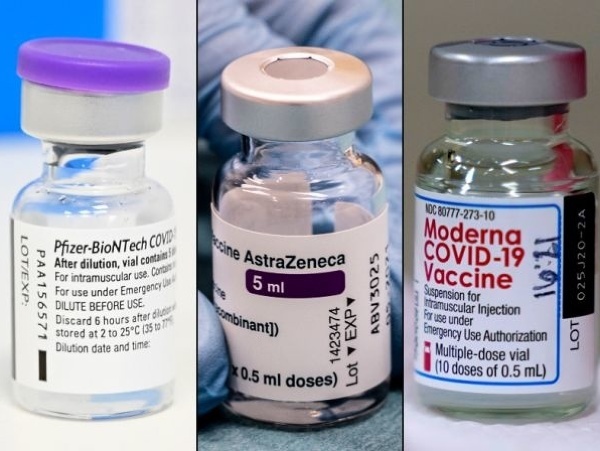
BRUSEL - Tento mesiac si bezpečnostný výbor agentúry EMA (PRAC) posvietil na množstvo bezpečnostných signálov týkajúcich sa vakcín COVID-19. "Vyhodnocovanie bezpečnostných signálov je bežnou súčasťou farmakovigilancie (veda a aktivity spojené s detekciou, posúdením, poznaním a prevenciou nežiaducich účinkov alebo iných liekových problémov, pozn. red.) a je nevyhnutné na zabezpečenie komplexných znalostí regulačných orgánov o výhodách a rizikách lieku," píše sa na stránke Európskej liekovej agentúry.
Vakcína Comirnaty od Pfizer/BioNTech môže spôsobovať v ojedinelých prípadoch opuch tváre. Preto PRAC odporučil zmeny informácií o tomto produkte.
KORONAVÍRUS Koniec očkovania AstraZenecou? Európska únia ju už viac nenakúpi!
Na základe prípadov hlásených do európskej databázy pre vedľajšie účinky, ale aj údajov z vedeckej literatúry výbor PRAC usúdil, že existuje prinajmenšom rozumná možnosť príčinnej súvislosti medzi vakcínou a hlásenými prípadmi opuchu tváre u ľudí s anamnézou injekcií s dermálnymi výplňami (mäkké, gélovité látky injikované pod kožu).
Výbor PRAC preto dospel k záveru, že opuch tváre u ľudí, ktorí majú v anamnéze injekcie s dermálnymi výplňami, by mal byť zahrnutý ako vedľajší účinok v príbalovom letáku. Pomer prínosu a rizika vakcíny zostáva nezmenený.
Krvné zrazeniny a vakcína Janssen
Výbor PRAC ukončil svoje hodnotenie vakcíny proti Covidu-19 Janssen od firmy Johnson & Johnson a potvrdil, to čo už bolo známe, že "výhody vakcíny v prevencii Covidu-19 prevažujú nad rizikami vedľajších účinkov".
Výbor 20. apríla odporučil ďalšie vylepšenie varovania pred trombózou (tvorbou krvných zrazenín v cievach) so syndrómom trombocytopénie (nízkych krvných doštičiek), ktoré bolo predtým uvedené v informácii o lieku pre vakcínu Janssen.
Informácie o výrobku budú po novom obsahovať aj odporúčanie, aby boli pacienti, ktorým je diagnostikovaná trombocytopénia do troch týždňov po očkovaní, aktívne vyšetrení na príznaky trombózy. Podobne sa má u pacientov, ktorí majú tromboembolizmus do troch týždňov po očkovaní, vyšetriť trombocytopénia.
"A nakoniec, trombóza so syndrómom trombocytopénie bude pridaná ako ´dôležité identifikované riziko´ do plánu riadenia rizík pre vakcínu. Držiteľ rozhodnutia o registrácii ďalej poskytne plán na ďalšie štúdium možných základných mechanizmov pre tieto veľmi zriedkavé udalosti," píše sa na stránke EMA.
Nevynechali ani Pfizer a Modernu
PRAC skúma kvôli zrazenínám aj vakcíny mRNA. Medzi ne patria očkovacie látky od Pfizeru/BioNTech a Moderny. Ale pri týchto vakcínach PRAC dospela k záveru, že bolo hlásených iba niekoľko prípadov krvných zrazenín s nízkym počtom krvných doštičiek.
"Z hľadiska vystavenia ľudí mRNA vakcínam sú tieto počty extrémne nízke a ich frekvencia je nižšia ako u ľudí, ktorí neboli očkovaní. Zdá sa, že navyše tieto prípady nepredstavujú špecifický klinický obrazec pozorovaný pri očkovaní vakcínami Vaxzevria (AstraZenca, pozn. red.) a Janssen (Johnson & Johnson, pozn. red.). Celkovo súčasné dôkazy nenaznačujú príčinnú súvislosť," uvádza sa na stránke EMA.
Ďalší možný vedľajší účinok vakcíny AstraZeneca
PRAC analyzuje údaje poskytnuté držiteľom rozhodnutia o registrácii o prípadoch Guillain-Barreovho syndrómu (GBS) hlásených po očkovaní. GBS je porucha imunitného systému, ktorá spôsobuje zápal nervov a môže mať za následok bolesť, necitlivosť, svalovú slabosť a ťažkosti s chôdzou. GBS bol identifikovaný počas procesu udeľovania povolenia na uvedenie na trh ako možný nežiaduci jav vyžadujúci špecifické monitorovanie bezpečnosti.
Zápal srdca a vakcína Comirnaty od Pfizeru
EMA si je vedomá prípadov myokarditídy (zápal srdcového svalu) a perikarditídy (zápal obalu srdcového svalu) hlásených hlavne po očkovaní Comirnaty. Momentálne nič nenasvedčuje tomu, že by tieto prípady boli spôsobené vakcínou.
Výbor PRAC však požiadal držiteľa rozhodnutia o registrácii, aby poskytol ďalšie podrobné údaje vrátane analýzy udalostí podľa veku a pohlavia v kontexte nasledujúcej súhrnnej správy o pandémii bezpečnosti a zváži, či sú potrebné ďalšie regulačné opatrenia.
Výbor PRAC navyše požiadal držiteľa rozhodnutia o registrácii pre vakcínu proti Covidu-19 Moderna - tiež vakcínu mRNA -, aby sledovala podobné prípady s ich vakcínami a poskytla tiež podrobnú analýzu udalostí v súvislosti s nasledujúcou súhrnnou správou o pandémii. "Keď budú k dispozícii nové informácie, agentúra EMA bude ďalej komunikovať," uzatvára EMA svoju správu.